|
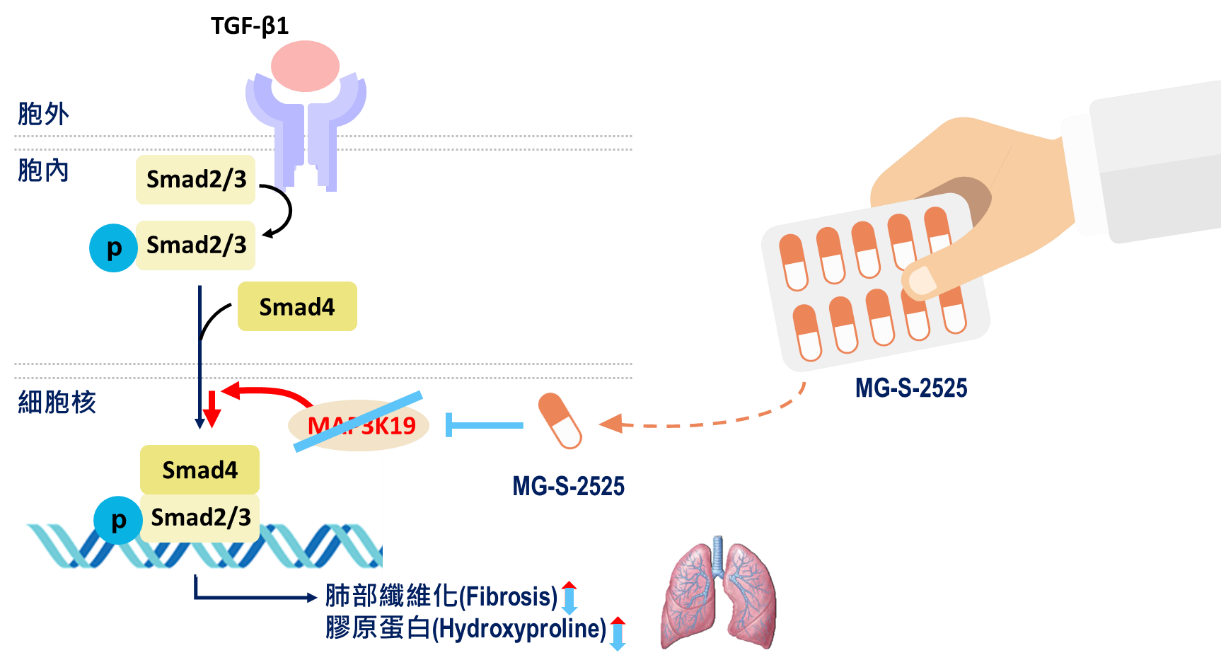
信力生技MG-S-2525新藥是MAP3K19小分子抑制劑,藉由降低肺部MAP3K19的表現量或活性可減緩相關的發炎反應,已取得美國FDA孤兒藥資格認定…… |
|
▌抑制TGF-β訊息傳遞路徑 有效降低促發炎細胞因子IL-6及IL-8表現 MG-S-2525為小分子新藥,是一個全新的口服抗發炎製劑,其有效成份HL0能透過抑制Mitogen-activated protein kinase 19 (MAP3K19)蛋白激酶,進而調控Transforming growth factor-β (TGF-β)訊息傳遞路徑,減緩肺部發炎反應。MG-S-2525新藥經由體外(In vitro)試驗結果發現MAP3K19蛋白激酶在Transforming growth factor-β (TGF-β)訊息傳遞路徑當中扮演一個非常重要的角色,而TGF-β訊息傳遞路徑常見於發炎反應相關的機制,亦是造成肺部纖維化的原因之一。MAP3K19蛋白激酶具有高度組織專一性,僅在肺臟之第二型肺泡細胞、間質巨噬細胞以及支氣管上皮細胞有表現,尤其在特發性肺纖維化(Idiopathic pulmonary fibrosis, IPF)和慢性阻塞性肺病(COPD)患者的肺臟組織中更有大量的MAP3K19表現。此外,在臨床前的動物試驗證實可有效降低促發炎細胞因子IL-6及IL-8的表現,對於因發炎所引起的非囊腫性纖維化支氣管擴張症(NCFB),具有相當大的治療潛力。
▌取得美國FDA孤兒藥資格、TFDA二期人體臨床試驗IPF項目許可 抗發炎製劑MG-S-2525小分子新藥於2018年12月取得美國食品藥物管理局(US FDA)特發性肺纖維化(IPF)孤兒藥資格認定(ODD),並於2019年8月在台北醫學院附設醫院完成一期人體臨床試驗,另外也於2021年3月12日取得TFDA二期人體臨床試驗IPF項目許可,預計於2022年完成二期人體臨床試驗。MG-S-2525新藥已取得台灣、美國、日本、澳洲等14國專利,部分國家尚在審查中,針對其作為特發性肺纖維化(IPF)之活性化學成分、調節COPD內調控激酶(RC激酶)的活性及應用於疾病治療等進行佈局。信力生技掌握肺部疾病醫療未被滿足需求,可提升病患的醫療品質,並擁有廣大國際商機。
▌技術強項與優勢
|
|
▌開放那些合作項目? 通過臨床驗證,即授權予生物技術、製藥合作夥伴,以推動新藥後期開發及商品化。區域授權或全球區域授權均可,依不同開發階段收取里程碑金和產品使用費等及資金投資合作。
|
Copyright © 2012 - 2024 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved