|
心臟血管疾病是全球人類死亡原因排名第一的疾病,每年因心臟血管疾病而死亡的人數高達一千七百多萬人之多。然而心臟的再生能力是非常有限的,心臟損傷後會導致不可逆的心肌細胞喪失,進而致使心臟衰竭,最終導致病患走向死亡。成大劉嚴文教授團隊研發「低免疫源性多能幹細胞分化的心肌細胞」,臨床前實驗研究結果顯示移植後,只需使用極低劑量免疫抑制劑即可維持移植細胞存活並修復心肌梗塞組織,可供異體細胞治療使用... |
|
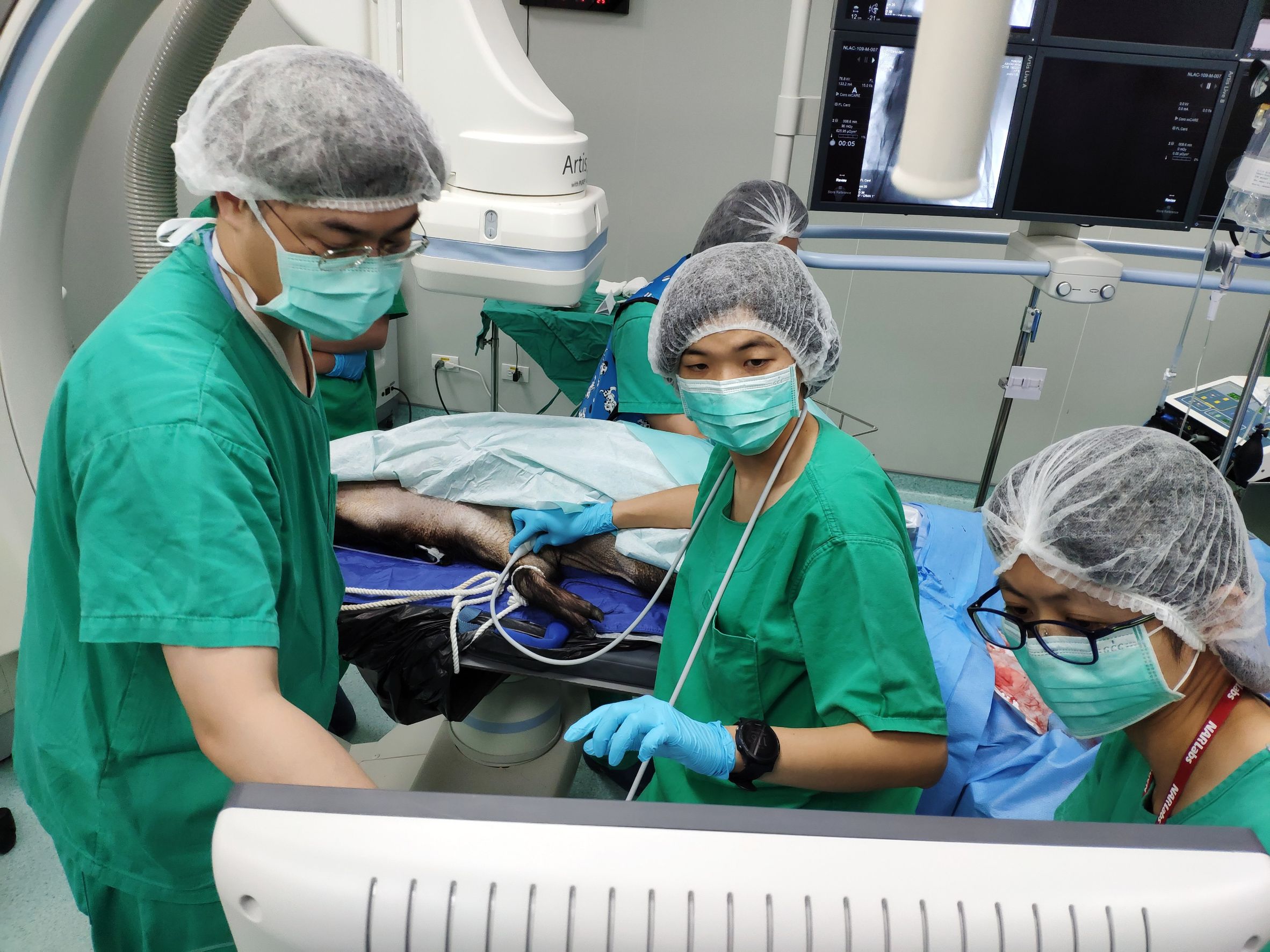
心臟血管疾病是全球人類死亡原因排名第一的疾病,每年因心臟血管疾病而死亡的人數高達一千七百多萬人之多。心肌梗塞以及其後遺症,例如: 心臟衰竭,則正是因心血管疾病而致死病例的主要原因。然而心臟的再生能力是非常有限的,心臟損傷後會導致不可逆的心肌細胞喪失,進而致使心臟衰竭,最終導致病患走向死亡。現今的醫療照護雖然可以大幅降低心肌梗塞與心衰竭的急性期死亡率,卻無法再生心的心臟肌肉細胞來修復因心肌梗塞而壞死的心臟部位。到目前為止,許多臨床試驗利用「成體幹細胞」來治療急性心肌梗塞,因成體幹細胞無法大量且有效地分化衍生出心臟肌肉細胞導致治療成效無法長久、甚至沒有療效。所以,在醫學上仍有這個相當重要卻未被滿足的需求。成大劉嚴文教授團隊研發「低免疫源性多能幹細胞分化的心肌細胞(HLA II-/HLA I+/HLA-E+/HLA-G+ iPSC)」,臨床前實驗研究結果顯示移植低免疫源性多能幹細胞分化的心肌細胞到動物心臟後,只需使用極低劑量免疫抑制劑即可維持移植細胞存活並修復心肌梗塞組織,可供異體細胞治療使用。 成大劉嚴文教授團隊以人類多能幹細胞分化心肌細胞突破自體誘導多能幹細胞限制 目前,器官或細胞移植在臨床應用上,仍有許多技術上的限制與缺陷。傳統醫學上認為使用自體體細胞重新編程(cell reprogramming)為誘導多能幹細胞(induced pluripotent stem cell, iPSC),再分化成特定組織進行自體移植治療的免疫排斥是最低並且是最直接與安全的方式。然而後續研究發現其限制包含: (1) 自體誘導多能幹細胞產製成本過高: (2) 無法用於急性症狀治療: (3) 免疫排斥反應: 成大劉嚴文教授團隊已證實移植人類多能幹細胞分化的心肌細胞可以修復大動物(獼猴、豬)心肌梗塞組織。然而,這些心肌細胞會引起免疫排斥反應。必須終身服用高劑量的抗排斥藥物,這卻會增加併發症,大大限制這類心肌細胞在臨床中的應用。
低免疫源性多能幹細胞分化心肌細胞讓異體移植患者不需服用高劑量免疫抑制劑 為突破移植所造成免疫排斥等相關臨床問題,成大劉嚴文教授團隊以先前研發成果為基礎,進一步發展「低免疫源性多能幹細胞分化的心肌細胞(hypoimmune-hiPSC-CMs)」作為異體移植治療材料,其主要特點是這些「低免疫源性多能幹細胞」以及「低免疫源性多能幹細胞分化的心肌細胞」並不表現第二型主要組織相容性抗原(major histocompatibility complex class II, MHCII),卻表現非典型性第一型主要組織相容性抗原(例如,HLA-E、HLA-G)等免疫調節基因,可以躲避宿主T細胞(CD4+)辨識以及抑制毒殺型T細胞(CD8+)與自然殺手細胞(NK cells)的活性,達到抗排斥的效果。此外,此細胞表現非典型第一型主要組織相容性抗原(HLA-E與HLA-G),能夠直接抑制CD8+ T細胞與自然殺手細胞活化,以多靶點的方式抑制移植後的免疫排斥。適合廣泛使用而不需等待冗長的基因配對時間。研究結果證實低免疫源性多能幹細胞分化的心肌細胞移植到齧齒類動物心肌梗塞處後,使用極低劑量免疫抑制劑即可維持移植細胞存活,修復心肌梗塞。 如前述,儘管使用自體體細胞重新編程為誘導多能性幹細胞,再分化成特定患部細胞進行自體移植同樣能夠達到治療效果,並且有較低的免疫排斥風險,但從取得病人體細胞至分化成特定組織細胞至少需半年至一年,並不適用於急症的病人上。由於「低免疫源性誘導多能幹細胞」透過「直接」躲避宿主免疫細胞辨識且抑制毒殺型免疫細胞的特性,而不須經由基因配對機制,可作為通用性醫療材料,能夠將大量培養的「低免疫源性誘導多能幹細胞」或其分化之特定組織(如: 心肌細胞)冷凍保存,能在疾病治療黃金時機立即解凍細胞給予移植治療。
※系列報導: |
| ※本文由生策中心新創幫編輯群採訪撰寫(口述:成大劉嚴文教授團隊 執筆:陳柏翔)。如有引用,請確實註明出處來源。 |
Copyright © 2012 - 2024 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved