|
鈦隼生物科技創辦人兼執行長陳階曉醫師在從醫後,體認到台灣醫材仰賴進口,國內生產的高階醫材價格高昂,且不一定完全適合市場需求,因此毅然決然投入高階醫材的研究開發及臨床手術驗證,盼藉由完成符合國際臨床需求標準之手術導引系統,使高階醫材產品與國際市場接軌... |
|
根據衛生福利部統計,2019年全國神經外科住院醫療申請人數共有103,511人。神經外科醫療費用約佔所有外科的22%,其中腦腫瘤相關疾病發生在55歲以上患者即佔51%,顯示人口老化伴隨的腦部之檢查與手術需求將大幅提升。然而,鈦隼生物科技創辦人兼執行長陳階曉醫師;在從醫後,體認到台灣醫材仰賴進口,國內生產的高階醫材價格高昂,且不一定完全適合市場需求,因此毅然決然投入高階醫材的研究開發及臨床手術驗證,盼藉由完成符合國際臨床需求標準之手術導引系統,使高階醫材產品與國際市場接軌,建立台灣在亞太區醫材研發中心的地位。 鈦隼科技透過研、產、製合一降低高階醫材市場門檻並拓展至臨床實證 陳階曉旁人的一句「台灣都只有代理商」,道盡目前國內高階醫材市場所遇到的現狀,滿懷想法的他,決定靠自己改變現況。 為了降低高階醫材導入門檻,鈦隼生物科技大部分軟硬體於國內研發及生產製造,因此在整套系統價格上具有相當的競爭優勢,讓更多醫療院所導入門檻降低,使更多病患受惠。 鈦隼生物科技在第一代產品NaoTrac開發完成後,已拓展臨床場域實證,於中國醫藥大與花蓮慈濟醫院進行多次臨床手術。而在花蓮慈濟醫院的臨床研究成果,更是登上歐洲知名醫學期刊《Acta Neurochirurgica》。
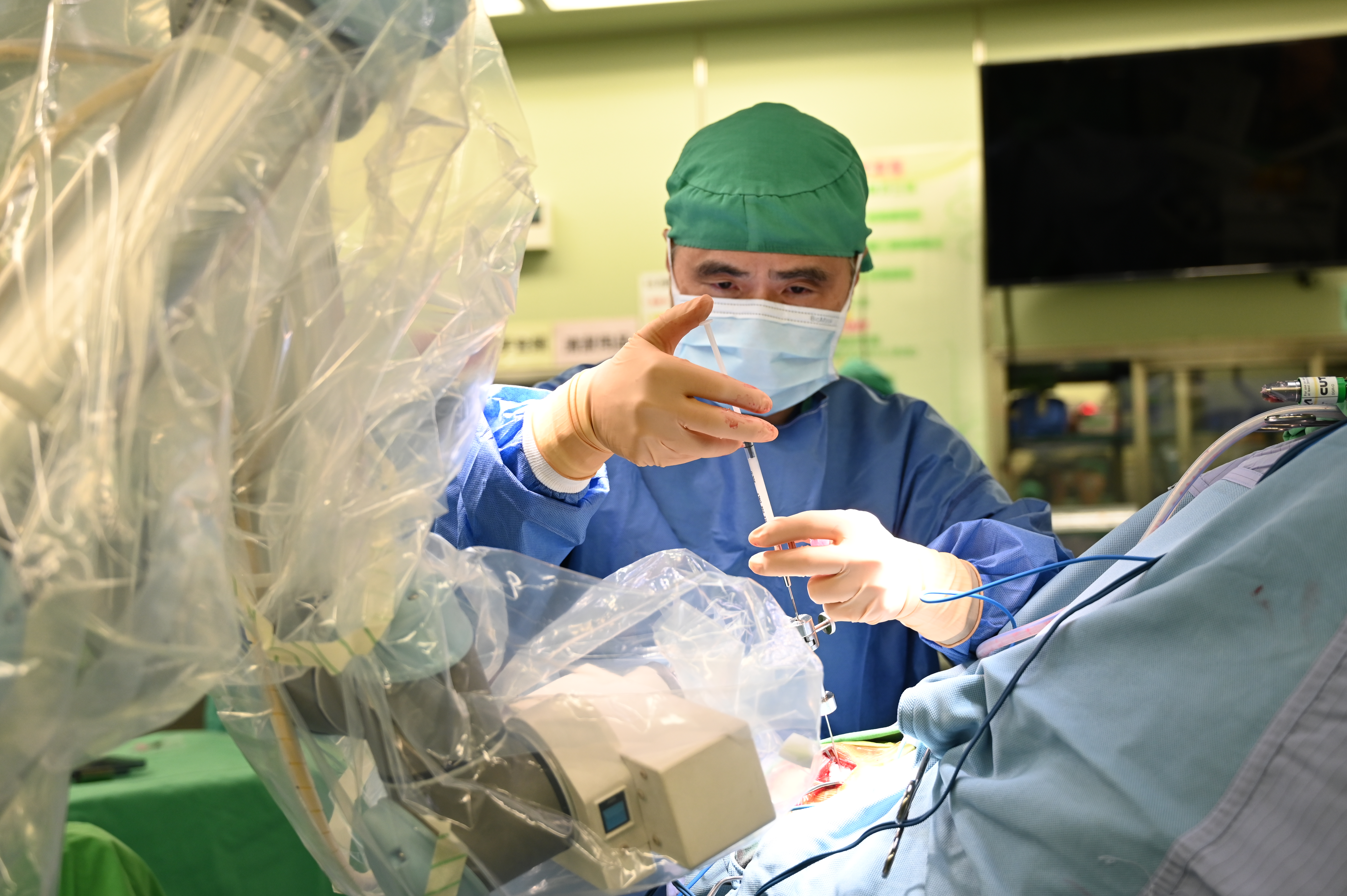
※NaoTrac手術導航機器人已拓展進入臨床場域實證。(地點: 花蓮慈濟醫院; 照片來源: 鈦隼生物科技) 獲歐盟CE與TFDA等多項許可 鈦隼生物科技瞄準第二代產品研發 鈦隼生物科技於今年8月時,在花蓮慈濟醫院進行臨床手術實況線上直播,邀請來自台、美、加、日、中、馬等多國執業醫師、醫材經銷商、醫學單位、投資者等眾多單位,展現該手術導航機器人的高準確度及高效率。
NaoTrac已陸續取得歐盟CE許可證以及台灣衛福部核准之醫療器材許可證,預計在2023年申請美國FDA醫療器材許可證,以及沙烏地阿拉伯SFDA醫療器材許可證等多國許可。 目前發展中的第二代產品將導航系統優化為AI自動化定位導航,並增加功能與介面,以應對術中各種突發狀況,例如: 自動偵測病患位置是否移動,並即時調整手術路徑、以及在術前或術中規劃出多條安全手術路徑,自動進行風險分析避開重要功能區域及主要血管。該系統未來也有望應用至骨科、脊髓、胸腔等外科手術,擴大實際臨床功能。 在陸續取得各國及區域的產品許可證後,該產品初期將以外銷或委託經銷商模式進行銷售,透過經銷商布建銷售通路,並以各大醫療院所為主要之銷售對象。未來則將計畫在歐美市場以品牌行銷為主,並吸引國際大廠合作。
※系列報導: |
| ※本文由生策中心新創幫編輯群採訪撰寫(口述:鈦隼生物科技 執筆:張家瑋)。如有引用,請確實註明出處來源。 |
Copyright © 2012 - 2025 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved