學研新創 - 生技製藥與精準醫療
以新穎融合蛋白促血管正常化以克服抗藥性及增強癌症免疫療法
2020-12-23
李岳倫副研究員團隊/財團法人國家衛生研究院癌症研究所
李岳倫、郭政良、柯泰名、周含諭、蔡瑞玲
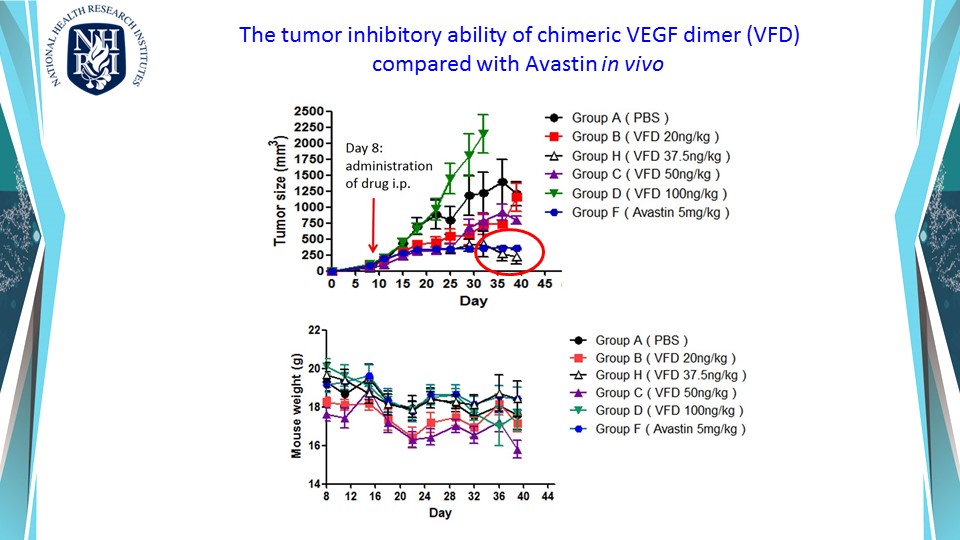
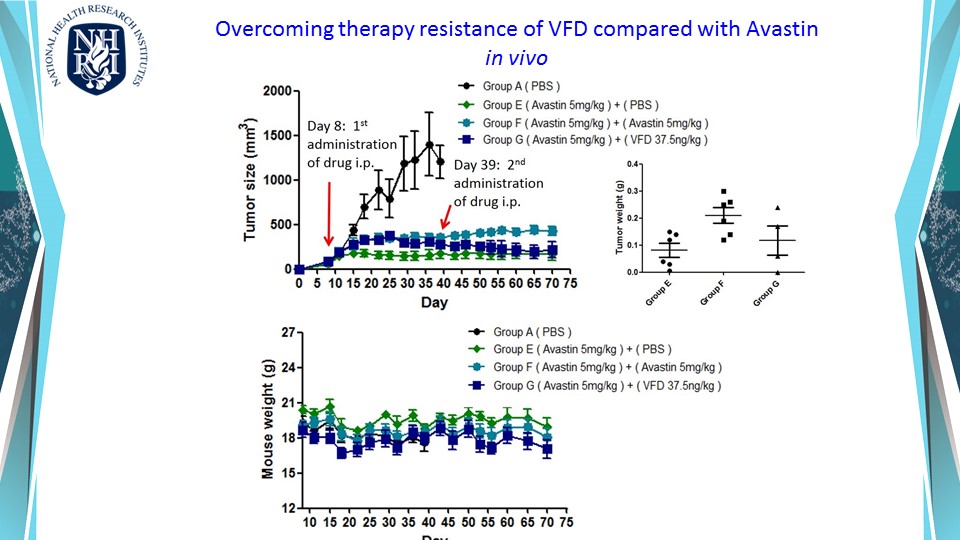
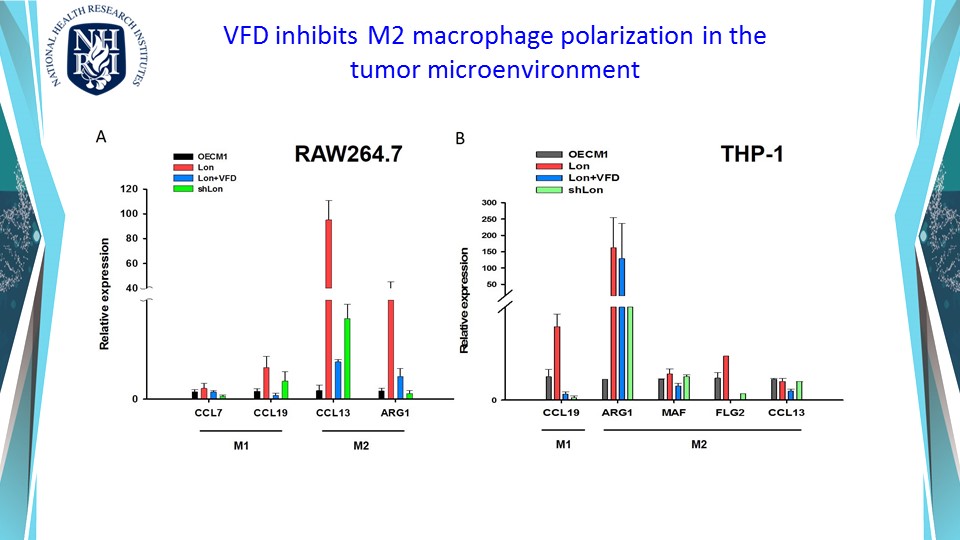
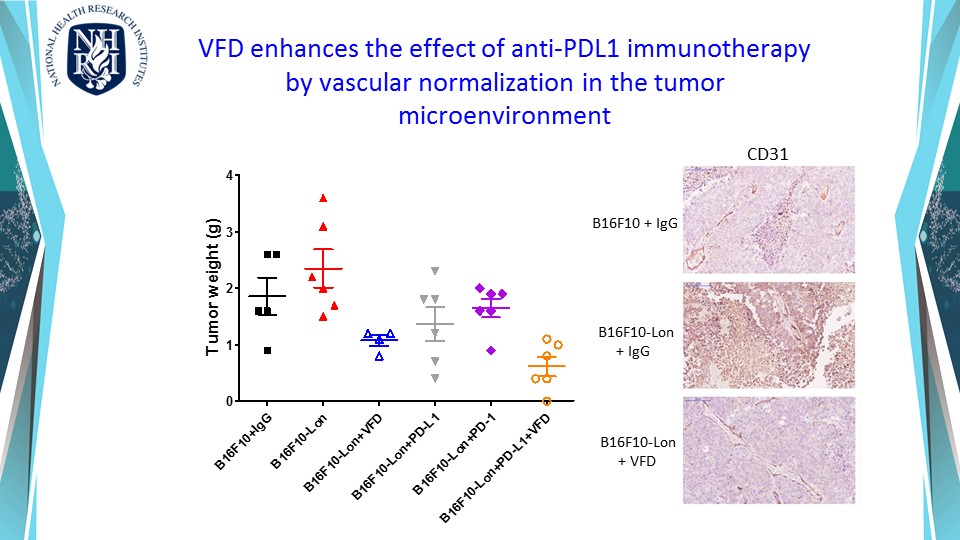
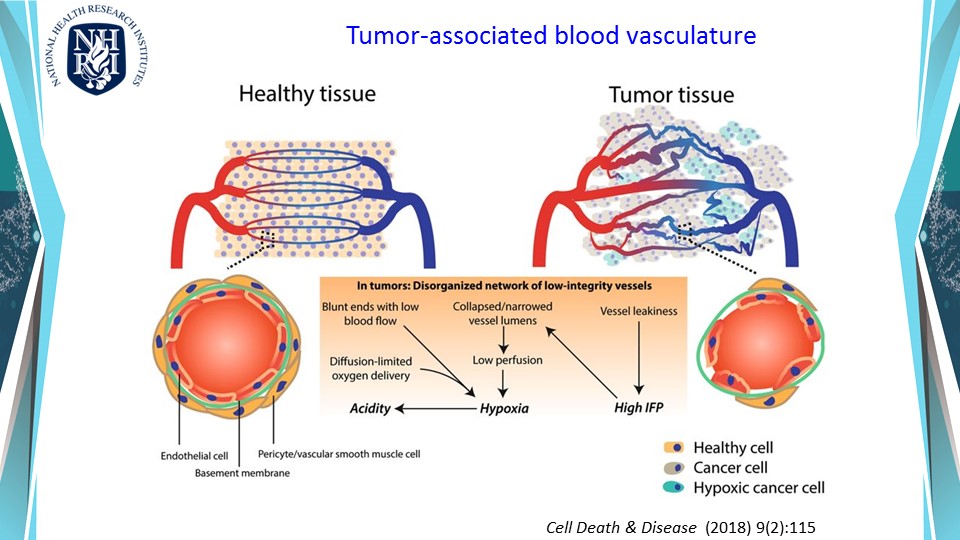
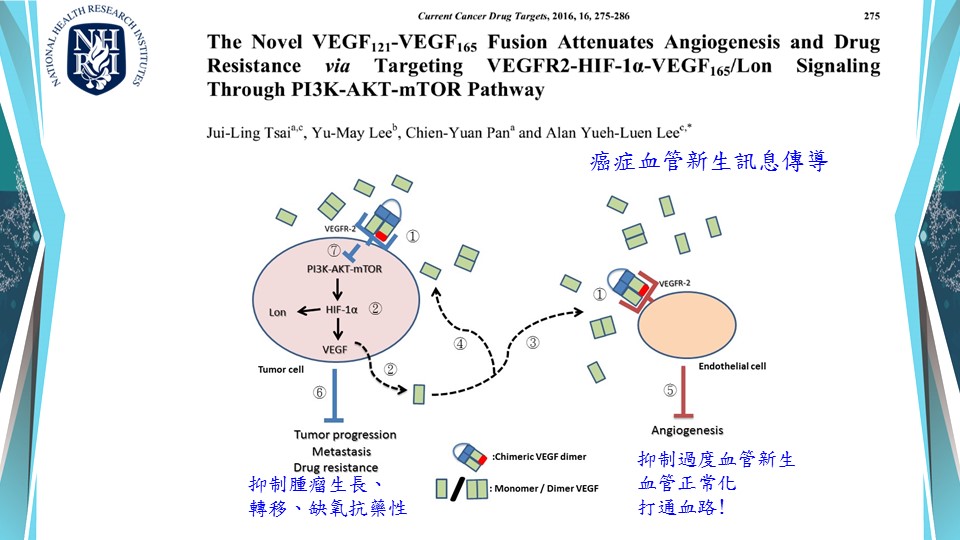
由於免疫治療已是癌症治療的明日之星,以血管正常化增加免疫細胞浸潤的策略,希望能增強免疫治療的合併治療效果。癌症血管新生是腫瘤在生長到相當程度大小時,因應缺乏養分、缺氧等壓力所發展出來的一種存活策略,同時也成為癌細胞轉移的管道。於是針對抑制血管生長因子 (VEGF-A) 的單株抗體藥物-癌思停 (Avastin/Bevacizumab),於 2004 年經美國FDA 核准問市。然而,癌思停很快就出現抗藥性,反而促進癌症病人轉移造成死亡。歸咎其原因,是治療後腫瘤組織因嚴重缺氧,出現代償作用而啟動其他生成機制所致。再者,腫瘤新生血管結構多扭曲且粗糙佈滿孔隙,極不利於藥物輸送與免疫細胞的浸潤。因此我們建構出新穎 VEGF121-VEGF165 融合蛋白,希望以血管正常化的思維,抑制血管內皮細胞的過度的血管新生,及同時抑制癌細胞代償作用。實驗結果顯示VEGF121-VEGF165合併anti-PD-L1可以更加有效抑制腫瘤在小鼠體內的生長,並且促使腫瘤內血管正常化,即以血管正常化來克服抗藥性及藉增加免疫細胞浸潤來增強癌症免疫療法。
技術優點:
(1) 抑制腫瘤細胞存活機制,避免因過度缺氧造成再復發,以降低抗藥性。
(2) 用極低濃度處理就可見顯著的抑制效果,可降低藥品的生產成本,也可避免蛋白藥物免疫過敏性的缺點。
(3) 此融合蛋白源自人類並且可以在人胚胎腎細胞中生產,將可增加藥物對人體的有效性、減少排斥性。
(4) 加入抗體的Fc區域,不僅可增強二聚體的結合,還可藉由Fc接受器來增強免疫細胞的活性,而且在結構上使得蛋白質的半衰期在體內更長、更趨穩定。
(5) 以血管正常化策略增加免疫細胞浸潤,以增加 anti-PD-L1的合併治療效果。
評審推薦
1.利用腫瘤血管增生機制,設計新形態藥物,開發之VEGF121-VEGF165 融合蛋白,可克服腫瘤細胞對抗癌藥產生之抗藥性,具創新性。
2.智財保護方面已有相當的佈局規劃,若能成功上市,具市場潛力。
2.智財保護方面已有相當的佈局規劃,若能成功上市,具市場潛力。
2022年度精進成果
本發明利用基因遺傳工程改造血管內皮細胞生長因子及抗體的Fc區域組成全新的Fc-VEGF融合抗體蛋白 (Fc-VFD)。此藥物可以低劑量抑制過度腫瘤血管增生與腫瘤生長,促使腫瘤內血管變為較正常,還可藉由免疫細胞表面的Fc接受器來活化免疫細胞,增強癌症免疫療法。此技術已獲得中華民國、美國、中國、歐洲以及日本專利。實驗結果證實,以Fc-VFD融合抗體蛋白處理後,可增加腫瘤微環境中殺手T細胞與自然殺手(NK)細胞的浸潤,在與anti-PD-L1的合併治療實驗中,可讓免疫治療效果更加顯著。結果已於2022年七月發表在國際知名期刊:癌症免疫學與免疫治療 (Cancer Immunology, Immunotherapy)。本發明已證實可抑制多種腫瘤生長,可以以低劑量搭配抗癌藥物或細胞免疫療法,將成為未來極具市場廣度潛力的增強癌症免疫療法!
團隊簡介

|
|||||||||
本網站中所有資料(包括影音.文字.圖表.數據等) ,均屬於本中心或各該新創企業團隊之專屬財產,如有引用,請確實註明出處來源。
<完整資訊>
財團法人生技醫療科技政策研究中心 版權所有
Copyright © 2012 - 2025 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved
Copyright © 2012 - 2025 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved