韓鴻志、林欣榮、邱紫文、周姵妏、劉人瑋
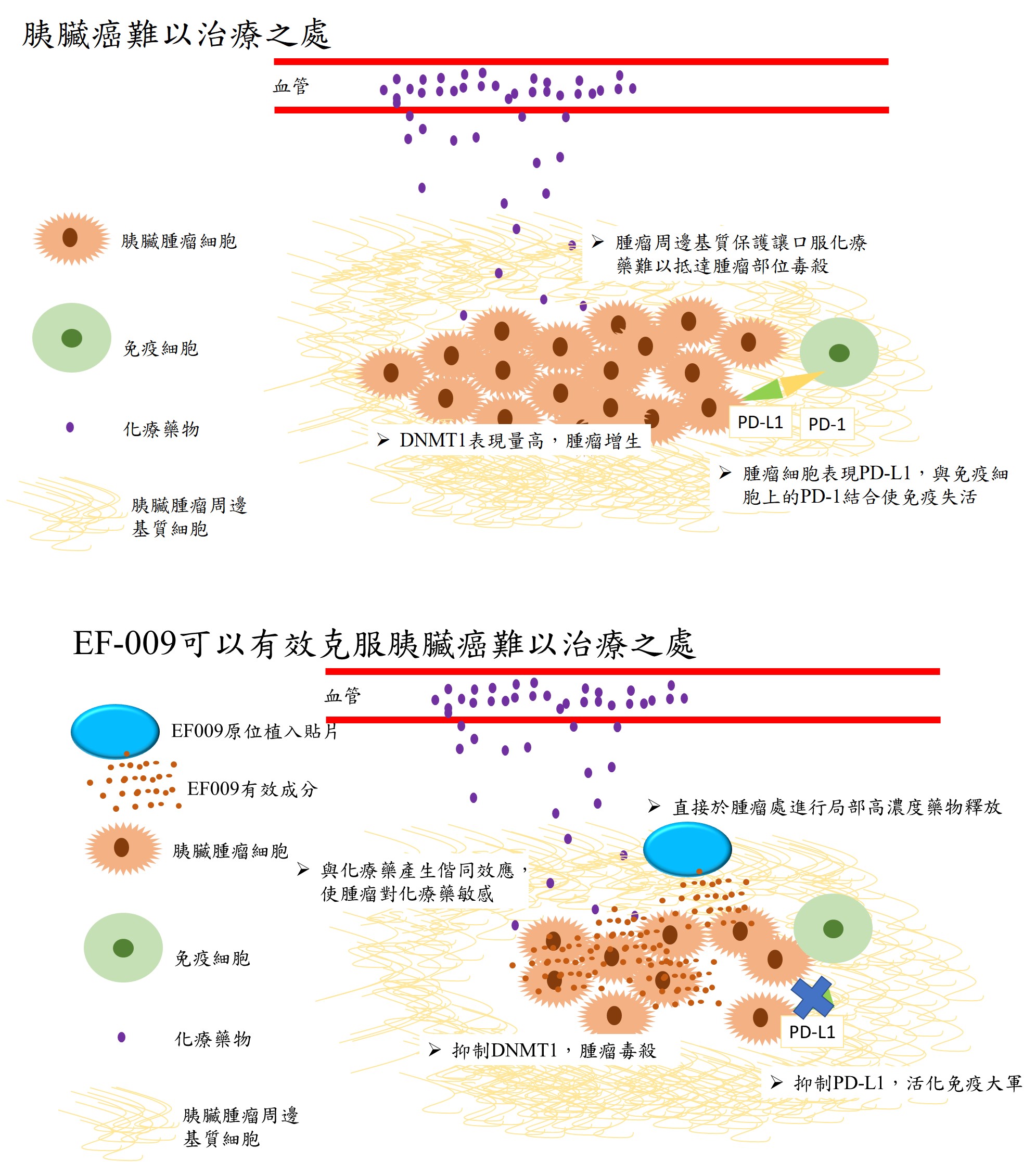
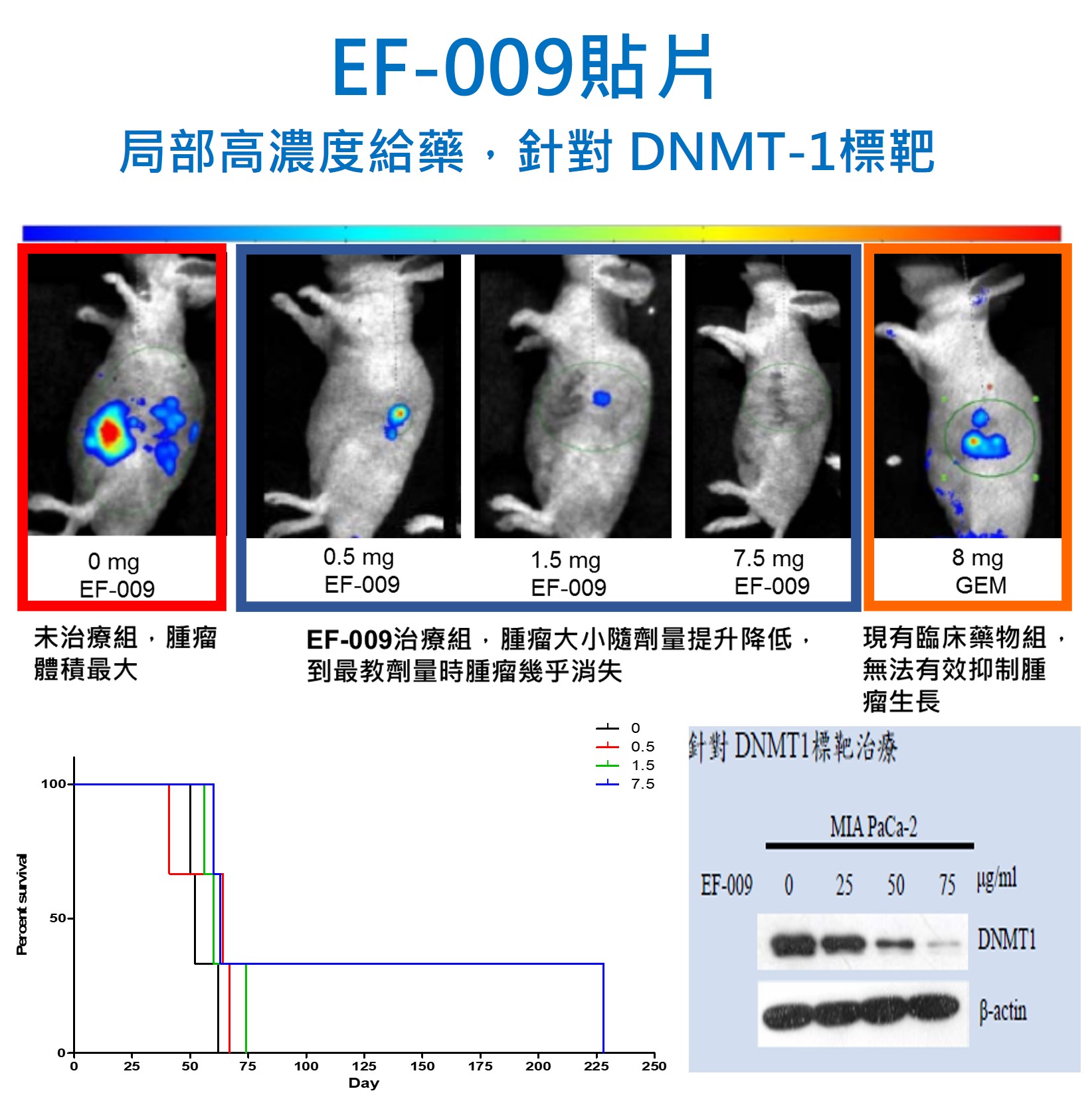
本開發案鎖定胰臟癌未滿足市場進行新藥 EF-009之開發。在 APPG Inquiry Pancreatic Cancer Research機構之統計,進30年來醫學的進展已使大部癌症之五年存活率提高至超過40%,然而胰臟癌五年存活率仍然僅5%,顯示市場上仍然缺少有效的胰臟癌藥物。而根據Global Information, Inc.之產業報告,全球胰臟癌2016年之市場規模為美金36.8億元,並預估以9.3%之CAGR持續成長。相較於臨床用藥 Gemcitabine 在過去試驗中約延長胰臟癌動物模式約2週之壽命,EF-009針對胰臟癌治療的動物試驗中,能夠有效延長試驗動物約6週之壽命,預估療效為現有藥物的3倍。且EF-00除了自身具有毒殺腫瘤細胞與腫瘤幹細胞的特性,更能夠與化療藥產生協同效應,並降低腫瘤細胞PD-L1表現,未來除了自身應用,也能夠與化療或是目前最流行的免疫療法進行搭配。目前 EF-009的臨床前期開發已完成,除了擁有符合 PIC/S GMP之原料藥、賦形劑、植入錠片製程外,EF-009之藥物毒性試驗、安全性藥理試驗、基因毒試驗、藥物動力學試驗亦有結果初步證實其安全性與藥物代謝特性。在此基礎下,技轉廠商長弘生技已完成美國食藥署與台灣衛服部的 IND (investigate new drug; 新藥臨床試驗許可)申請與核准,並將著手進行後續新藥開發,依序完成Phase I、II、III期臨床試驗,以邁向本土開發之新藥上市為最終目標。
2.許多癌症中,DNA methyltransferase (DNMT)家族的蛋白質表現量常有增加的趨勢,且臨床上也發現DNMT1 表現量較高的病人預後存活率較差,本開發案鎖定未滿足市場進行之開發。

|
|||||||||
Copyright © 2012 - 2024 Research Center for Biotechnology and Medicine Policy (RBMP). All Rights Reserved